Ang valency ng carbon ay ... (numero). Samakatuwid, kapag nagsusulat ng mga pormula sa istruktura, ang apat na gitling na naglalarawan ng mga bono ng kemikal ay dapat umalis sa carbon.
Form ng pagpasok ng komposisyon organikong molekula, kung saan ang bawat C atom ay ipinapakita nang hiwalay na may mga bono, ay tinatawag na may………. f…….. . Ang mga atomo ng carbon na nakagapos ng kemikal ay kalansay ng carbon mga molekula ng sangkap.
Tatlong uri ng mga pormula sa istruktura
1. Ang pinakakumpletong anyo ng hydrocarbon formula ay kapag ang bawat atom ng molekula ay ipinapakita nang hiwalay:
Ang nasabing rekord ay napakalaki, tumatagal ng maraming espasyo at bihirang ginagamit.
2.
Ang anyo ng talaan, na nagpapahiwatig kabuuang bilang hydrogen atoms sa bawat C atom, at ang mga gitling ay inilalagay sa pagitan ng mga katabing carbon,
ibig sabihin x…….may…. :
CH 3 -CH 2 -CH 3, Cl-CH 2 -CH 2 -Br.
3. Isang structural formula kung saan ang mga gitling sa pagitan ng mga atomo na matatagpuan sa parehong linya sa talaan ay hindi ipinahiwatig, habang ang mga atom na papunta sa iba pang mga linya ay konektado ng mga gitling sa isang tuwid na kadena:
Minsan ang mga carbon chain ay ipinapakita bilang mga sirang linya, mga geometric na hugis(tatsulok, parisukat, kubo). Kasabay nito, sa bawat break ng chain, pati na rin sa simula at sa dulo ng chain, isang C atom ang ipinahiwatig. Halimbawa, ang mga imahe
tumutugma sa mga pormula sa istruktura
Nasa ibaba ang ilang katangian ng mga indibidwal na saturated hydrocarbon at ang anyo ng kanilang pagtatala (Talahanayan 1).
Talahanayan 1
Mga pangalan ng saturated hydrocarbons (alkanes) ng isang linear na istraktura
| Pangalan alkane | Molekular pormula | Structural pormula | Pinagsama-sama kundisyon | Temperatura punto ng kumukulo, °C |
|---|---|---|---|---|
| Methane | CH 4 | CH 4 | Gas | –161,6 |
| Ethane | C 2 H 6 | CH 3 CH 3 | Gas | –88,6 |
| Propane | C 3 H 8 | CH 3 CH 2 CH 3 | Gas | –42,1 |
| Butane | C 4 H 10 | CH 3 CH 2 CH 2 CH 3 | Gas | –0,5 |
| Pentane | C 5 H 12 | CH 3 (CH 2) 3 CH 3 | likido | 36,1 |
| Hexane | C 6 H 14 | CH 3 (CH 2) 4 CH 3 | likido | 68,7 |
| Heptane | C 7 H 16 | CH 3 (CH 2) 5 CH 3 | likido | 98,5 |
| Octane | C 8 H 18 | CH 3 (CH 2) 6 CH 3 | likido | 125,6 |
| Nonan | C 9 H 20 | CH 3 (CH 2) 7 CH 3 | likido | 150,7 |
| Dean | C 10 H 22 | CH 3 (CH 2) 8 CH 3 | likido | 174,0 |
Pangalan ng branched at substituted alkanes
1. Ang pangunahing carbon chain ay pinili at binibilang sa paraang (kaliwa o kanan) na ang mga papasok na substituent ay tumatanggap ng pinakamaliit na numero.
2. Nagsisimula ang pangalan sa isang digital locant - ang carbon number kung saan matatagpuan ang substituent. Pagkatapos ng numero, ang pangalan ng kinatawan ay nakasulat sa pamamagitan ng gitling. Ang iba't ibang mga substituent ay nakalista nang sunud-sunod. Kung ang parehong mga substituent ay paulit-ulit nang dalawang beses, pagkatapos ay sa pangalan pagkatapos ng mga digital na locant na nagpapahiwatig ng posisyon ng mga substituent na ito, ang prefix na "di" ay nakasulat. Alinsunod dito, na may tatlong magkatulad na mga substituent, ang prefix ay "tatlo", na may apat - "tetra", na may limang substituents - "penta", atbp.
Mga pangalan ng mga kahalili

3. Kasama ng prefix at substituent, isinusulat nila ang pangalan ng hydrocarbon na binibilang bilang pangunahing carbon chain:
a) 2-methylbutane; b) 2,3-dimethylpentane; c) 2-chloro-4-methylpentane.
Ang mga pangalan ng cycloalkanes ay magkatulad, tanging ang prefix na "cyclo" ay idinagdag sa pangalan ng hydrocarbon - ayon sa bilang ng mga carbon atom sa cycle:
Ang mga sangkap na magkatulad sa istraktura, ngunit naiiba ng isa o higit pang mga grupo -CH 2 -, ay kilala bilang g ....... .
Mga halimbawa homologues:
CH 3 -CH 3, CH 3 -CH 2 -CH 3, CH 3 -CH 2 -CH 2 -CH 3.
Ang elemento ng pagkakatulad ay ang mga alkanes na may linear na kadena:
Ang pagkakapareho ng tatlong mga formula ng mga sangkap ng huling halimbawa - sa bawat kaso, ang pangalawang C atom ng pangunahing carbon chain ay may parehong substituent - ang CH 3 group.
Ang kababalaghan ng pagkakaroon ng mga sangkap na naiiba sa istraktura at mga katangian, na may parehong husay at dami ng komposisyon, ay tinatawag at ....... .
Mga sangkap na may parehong m........... formula, ngunit naiiba sa………. ang mga formula ay...
(Talahanayan 2).
talahanayan 2
Mga halimbawa ng isomeric hydrocarbons
| Molecular formula | Mga istrukturang formula |
|---|---|
| C 4 H 10 | CH 3 CH 2 CH 2 CH 3, |
| C 5 H 12 | CH 3 CH 2 CH 2 CH 2 CH 3, |
| C 6 H 14 | CH 3 (CH 2) 4 CH 3, 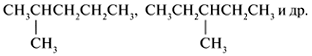
|
Mga panuntunan para sa pag-compile ng mga isomer sa halimbawa ng tambalang C 5 H 11 Cl.
1. Sumulat ng linear carbon chain C 5:
S-S-S-S-S.
2. Tukuyin kung saang klase ng mga hydrocarbon kabilang ang ibinigay na tambalan. Ang pagpapasiya ay ginawa gamit ang mga pangkalahatang formula para sa mga hydrocarbon ng iba't ibang klase (C n H2 n+2 , C n H2 n atbp.). Ang substance C 5 H 11 Cl ay chloroalkane, i.e. ay isang alkane derivative ng type C n H2 n+2 (n= 5), kung saan ang isang H atom ay pinalitan ng Cl. Nangangahulugan ito na ang lahat ng mga bono sa molekula ay iisa at walang mga cycle.
3. Ang mga C atom ng carbon chain (carbon skeleton) ay binibilang at ang isang Cl heteroatom ay inilalagay sa C-1:
4. Isulat ang kinakailangang bilang ng hydrogen atoms sa bawat carbon ng chain, dahil ang valency ay C - IV. Ang resulta ay isomer a):
![]()
5. Ang chlorine atom ay inililipat kasama ang pangunahing C 5 chain, sunud-sunod na ikinokonekta ito sa C-2 at C-3 atoms. Ito ay kung paano ang mga isomer b) at c) ay nakuha:
Ang karagdagang paglipat ng chlorine sa kanan kasama ang kadena ng mga bagong isomer ay hindi nagbibigay. Kaya, ang isomer a*) ay magkapareho sa isomer a), ang isomer b*) ay magkapareho sa isomer b). Sa mga isomer a *) at b *) nagbabago ang direksyon ng pag-numero ng C atoms, ang bilang ay mula kanan pakaliwa (nang walang mga asterisk ito ay mula kaliwa hanggang kanan):
6. Batay sa carbon skeleton (tingnan ang talata 3), ang sukdulan (ikalima) C atom ay pinunit at inilagay bilang isang substituent sa panloob na carbon ng chain (una sa C-2, pagkatapos ay sa C-3). Ang mga pangunahing chain ng C 4 ay nakuha na may isang carbon substituent sa C-2 at C-3:
Isulat ang mga pormula ng istruktura ng mga bagong isomer:
7. Sa pamamagitan ng paglalagay ng chlorine sa panloob na C atoms ng pangunahing C 4 carbon chain, dalawang karagdagang isomer ang nakuha:
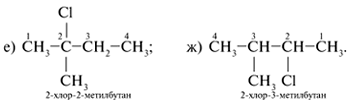
8. Ang isang substance ng formula C 5 H 11 Cl ay maaaring magkaroon ng tatlong-carbon na pangunahing kadena C 3:

Kaya, para sa isang sangkap na may molecular formula C 5 H 11 Cl, walong istruktural na formula ng mga isomer a)–h), na magkakaiba sa istraktura, ay maaaring tipunin.
1. Anong mga hydrocarbon ang tinatawag na unsaturated at paano sila nahahati? Sumulat ng mga pangkalahatang formula unsaturated hydrocarbons.
Ang mga unsaturated hydrocarbon ay ang mga naglalaman ng isa o higit pang maramihang mga bono. Ang mga pangunahing klase ng unsaturated hydrocarbons ay: alkenes, alkynes, at alkadienes.
2. Kasama sa mga alkenes ang:
3)
3. Batay sa mga kontemporaryong ideya tungkol sa mga orbital ng elektron, kilalanin ang likas na katangian ng mga bono ng kemikal sa molekula ng ethylene. 
4. Ang bilang ng mga σ-bond sa isang ethylene molecule ay:
2) 5
5. Anong mga uri ng isomerism ang nakikita sa saturated at unsaturated hydrocarbons? 
6. Iguhit ang mga pinaikling pormula ng istruktura ng lahat ng hydrocarbon na ang molecular formula ay . Pangalanan ang mga compound na ito. 
7. Bakit mas malaki ang bilang ng mga isomer para sa hydrocarbons ng ethylene series kaysa sa saturated hydrocarbons? Para sa patunay, magbigay ng mga isomer ng hydrocarbon na may mga molecular formula at . 
8. Ang isomer ng pentene-1 ay
3) 2-methylbutene-1
9. Propene homologue ay
1) butene-1
10. Paano nakukuha ang ethylene at hydrocarbons ng ethylene series? Isulat ang mga equation para sa mga katumbas na reaksyon. 
11. Ano ang mga kemikal na katangian ng ethylene at ang mga homologue nito? Suportahan ang iyong sagot gamit ang kaukulang mga equation ng reaksyon. 
 12. Isulat ang mga equation para sa mga reaksyon ng pagkasunog ng ethylene at propylene at ang kanilang pakikipag-ugnayan sa bromine water at isang solusyon ng potassium permanganate.
12. Isulat ang mga equation para sa mga reaksyon ng pagkasunog ng ethylene at propylene at ang kanilang pakikipag-ugnayan sa bromine water at isang solusyon ng potassium permanganate. 
13. Paano tumutugon ang propylene at butenes sa hydrogen halides? Gamitin ang mga halimbawang ito upang ipaliwanag ang kakanyahan ng panuntunan ni Markovnikov. 
14. Para sa anong mga layunin ginagamit ang ethylene at propylene?
Ang ethylene ay ginagamit upang makagawa ng ethylene glycol, polyethylene, at ethyl alcohol. Bilang karagdagan, ang ethylene ay nagpapabilis sa pagkahinog ng prutas. Ang isopropyl alcohol at polypropylene ay nakuha mula sa propylene.
15. Anong mga reaksyon ang tinatawag na polymerization reactions? Isulat ang equation ng reaksyon para sa polimerisasyon ng propylene. 
16. Gumawa ng mga Equation mga reaksiyong kemikal nagpapatunay genetic na koneksyon sa pagitan ng mga klase mga organikong compound sa diagram 5. 
 Gawain 1. Kalkulahin:
Gawain 1. Kalkulahin:
a) anong dami at anong masa ng ethylene ang maaaring makuha mula sa 160 ml ng ethyl alcohol, ang density nito ay 0.8 g/cm3; b) anong dami ng absolute (anhydrous) ethyl alcohol (ρ=0.8 g/cm3) ang makukuha mula sa 100 m3 ng ethylene (N.O.) 
 Suliranin 2. Kapag dumaraan sa ethylene tubig na bromine ang masa ng solusyon ay tumaas ng 7 g. Anong volume ng gas ang nag-react at anong masa ng 1,2-dibromoethane ang nabuo (n.o.)?
Suliranin 2. Kapag dumaraan sa ethylene tubig na bromine ang masa ng solusyon ay tumaas ng 7 g. Anong volume ng gas ang nag-react at anong masa ng 1,2-dibromoethane ang nabuo (n.o.)? 
Gawain 3. Anong volume ng ethylene (N.O.) ang kakailanganin para makakuha ng 126 kg ng ethylene oxide, kung mass fraction Ang pagkawala ng produksyon ng ethylene ay 0.1? 
Gawain 4. Anong volume ng hangin ang kailangan para masunog ang 50 litro ng propylene (n.o.s.)? 
1. Isulat ang mga pormula ng istruktura ng mga isomer ng mga carbonyl compound na may pangkalahatang formula na c5h10o at pangalanan ang mga ito ayon sa rational nomenclature, iupak nomenclature.
Desisyon:
Para sa mga carbonyl compound, ang pagbuo istruktura isomer ay nauugnay sa isang pagbabago sa istraktura ng carbon chain, isang iba't ibang kaayusan ng carbonyl group sa carbon chain:
Ang functional group sa mga structural formula ng aldehydes ay madalas na nakasulat sa anyo ng isang pinaikling formula bilang CHO (COH - mali!), Sa ketones, ang oxygen atom ay inilalagay sa panaklong (O).
2. Isulat ang mga equation para sa mga reaksyon ng oksihenasyon na may pinaghalong chromium ng butanal at 2-methylpentanone-3.
Desisyon:
Kapag ang mga aldehydes ay na-oxidized, ang mga carboxylic acid ay nabuo nang hindi binabago ang bilang ng mga carbon atom sa kanilang komposisyon. Ang oksihenasyon ng mga ketone ay sinamahan ng pagkasira ng carbon chain, na nagreresulta sa pagbuo ng isang halo ng mga carboxylic acid at (o) mga ketone na may mas maliit na bilang ng mga carbon atoms (kumpara sa orihinal na ketone) sa kanilang komposisyon:

3. Isulat ang mga scheme ng reaksyon ng acetone at acetaldehyde na may hydrocyanic acid, hydroxylamine. Ihambing ang reaktibiti ng mga carbonyl compound sa mga reaksyong ito.
Desisyon:
Ang pakikipag-ugnayan ng acetone at acetaldehyde sa mga reagents na ito ay tinutukoy bilang nucleophilic addition reactions (AN). Ang mga scheme ng reaksyon ay ganito ang hitsura:
a) pakikipag-ugnayan sa hydrocyanic acid


Ang hydrolysis ng mga nagresultang oxynitriles ay sinamahan ng pagbuo ng α - hydroxy acid, at ang bilang ng mga carbon atom sa komposisyon ng acid ay tumataas ng isa: 2-hydroxypropanoic acid
(lactic acid)
b) pakikipag-ugnayan sa hydroxylamine:

Ang mga reaksyon sa pagdaragdag ng nucleophilic na may mga nucleophile na naglalaman ng nitrogen (NH 3 , NH 2 OH, NH 2 -NH 2, atbp.) ay sinusundan ng pag-aalis ng molekula ng tubig mula sa produkto ng reaksyon.
Ang reaktibiti ng aldehydes sa mga reaksyong ito ay mas mataas kaysa sa mga ketone, dahil ang halaga ng positibong singil sa carbon atom ng carbonyl group sa aldehydes ay mas malaki kaysa sa ketones:
|
|
|
4. Kumuha ng acetone sa lahat ng posibleng paraan.
Desisyon:
Ang mga carbonyl compound ay maaaring makuha bilang resulta ng mga sumusunod na pagbabago:
1. hydrolysis ng 33 em-dihalogen derivatives ng hydrocarbons:

2. oksihenasyon ng mga alkohol, habang ang mga aldehydes ay nabuo mula sa mga pangunahing alkohol, at ang mga ketone mula sa mga pangalawang:

3. ozonolysis ng mga alkenes na sinusundan ng hydrolysis:

4. hydration ng alkynes (reaksyon ng Kucherov):

5. pyrolysis ng calcium (barium) salts ng carboxylic acids:
3.3. Mga carboxylic acid at ang kanilang mga derivatives
Panitikan
1. Ivanov, V.G. Organikong kimika: pag-aaral. allowance para sa mga unibersidad / V.G. Ivanov, V.A. Gorlenko. - M .: Publishing Center "Academy", 2009. -S. 222-254,469-479.
2. Grandberg, I.I. Organikong kimika: aklat-aralin. para sa mga unibersidad / I.I. Grandberg. - M.: Bustard, 2002. -S. 357-392, 410-426, 393-399.
3. Artemenko, A.I. Organikong kimika: aklat-aralin. para sa mga unibersidad / A.I. Artemenko. - M.: graduate School, 2009. -S.170-199, 251-253, 259-272, 402-408.
4. Petrov, A.A. Organikong kimika: aklat-aralin. para sa mga unibersidad / A.A. Petrov. - St. Petersburg: Ivan Fedorov, 2002. -S. 189-2003, 207-220, 257-285, 421-434.
Ang mga inirerekomendang aklat-aralin ay naglalaman ng mas maraming materyal kaysa sa kinakailangan ng programa. Ang lahat ng mga aklat-aralin ay nakikitungo nang detalyado sa elektronikong istraktura, mga kemikal na katangian ng mga carboxylic acid, ang paghahanda at paggamit ng mga acid at ang kanilang mga derivatives. Sa inirekumendang aklat-aralin, ang materyal ay ipinakita nang sistematiko at maigsi, samakatuwid mas mahusay na pag-aralan ang paksang "Mga carboxylic acid at ang kanilang mga derivatives" sa iyong sarili gamit ang isang aklat-aralin.
Ang mga derivatives ng hydrocarbons na naglalaman ng carboxyl group ay tinatawag na carboxylic acids.
Ang pag-aaral ng mga carboxylic acid ay dapat magsimula sa isang pagsasaalang-alang sa pangkat ng carboxyl at ang pangkalahatang pag-uuri ng mga acid. Depende sa likas na katangian ng radikal at ang bilang ng mga pangkat ng carboxyl, mayroong ilang mga uri ng mga carboxylic acid: aliphatic at aromatic carboxylic acid, mono- at dicarboxylic acid, pati na rin ang may halo-halong mga function - hydroxy-, oxo-, amino acids.
Kapag pinag-aaralan ang nomenclature, dapat tandaan na ang pinakakaraniwan ay ang mga maliit na pangalan ng mga acid, ang ilang mga pangalan ay dapat tandaan: acetic (ethanoic), butyric (butanoic), oleic, stearic, linoleic, tartaric, oxalic, atbp. Ang mga prinsipyo para sa pagbibigay ng pangalan sa mga acid ayon sa IUPAC nomenclature ay tinalakay kanina (tingnan ang "Nomenclature of organic compounds").
Kapag nag-aaral pisikal na katangian carboxylic acids, ang pansin ay dapat bayaran sa pagbuo ng intermolecular hydrogen bonds.
Kapag nag-aaral mga katangian ng kemikal ang mga acid ay dapat magtatag ng pagkakatulad sa mga inorganic acid: ang kakayahang maghiwalay, ang pagbuo ng mga asing-gamot. Ang pagkakaroon ng isang mobile hydrogen atom sa komposisyon ng carboxyl group -COO H tumutukoy mga katangian ng acid mga carboxylic acid. Ang lakas ng mga acid ay nakasalalay sa isang bilang ng mga kadahilanan: ang istraktura at komposisyon ng radical, ang pagkakaroon ng mga electron-withdraw o electron-donor na mga grupo sa radical, ang bilang ng mga carboxyl group, atbp. Bilang resulta ng pakikipag-ugnayan sa mga metal, metal oxide, base at ilang asin, ang mga acid ay bumubuo ng mga asin. Dapat mong isaalang-alang ang mga katangian ng sodium at calcium salts (solubility, attitude to hydrolysis, heating), bigyang-pansin ang mga salts ng mas mataas na carboxylic acids (soaps).
Ang mga carboxylic acid ay nailalarawan sa pamamagitan ng mga reaksyon ng pagpapalit ng nucleophilic. Ang pagpapalit ng hydroxyl group sa komposisyon ng carboxyl group ay humahantong sa paggawa ng mga acid derivatives: anhydride, acid halides, amides, esters. Dapat bigyang-pansin ng mag-aaral ang reaksyon ng esteripikasyon (pagkuha mga ester), kundisyon at mekanismo nito. Kapag pinag-aaralan ang kimika ng mga taba, kinakailangang kabisaduhin ang mga formula ng limang pangunahing acids (2 nililimitahan at 3 unsaturated) at trihydric alcohol - glycerol, na bahagi ng triglyceride. Dapat mong matutunan kung paano magsulat ng mga equation para sa mga reaksyon ng pagbuo ng taba, alamin ang pinakamahalagang kemikal na katangian ng mga taba: hydrolysis, hydrogenation.
Ang isang karaniwang pag-aari ng lahat ng mga derivatives ng mga acid ay ang kanilang hydrolysis (acidic at alkaline), na nagreresulta sa pagbuo ng isang carboxylic acid o asin nito. Ang mga acid derivatives ay malawakang ginagamit sa organic synthesis para sa acylation ng mga alcohol, phenols, amines, at iba pang compounds.
Kapag nag-aaral ng mga dicarboxylic acid, kinakailangang tandaan ang parehong pagkakapareho at pagkakaiba sa mga monocarboxylic acid, dahil sa malaking bilang ng mga pangkat ng carboxyl, ang kanilang impluwensya sa isa't isa.
Kapag pinag-aaralan ang istraktura at mga kemikal na katangian ng mga unsaturated acid, kinakailangang ulitin ang naunang pinag-aralan na materyal sa unsaturated hydrocarbons (tingnan ang "Alkenes").
Kapag nag-aaral ng mga hydroxy acid, dapat bigyang pansin ang optical isomerism na katangian ng mga compound na ito, upang isaalang-alang ang mga katangian ng mga acid sa mga tuntunin ng pangkat ng carboxyl (pagbuo ng mga asing-gamot, ester) at ang pangkat ng alkohol (pagpapalit ng pangkat ng OH, pagbuo ng alcoholates, eter at ester). Kinakailangang isaalang-alang ang ratio ng mga hydroxy acid sa pagpainit, ang pag-aalis ng tubig na may pagbuo ng mga produkto ng iba't ibang mga istraktura.
Ang mga keto acid ay maaaring isaalang-alang sa halimbawa ng pyruvic at acetoacetic acid. Pyruvic acid ay ang pinakamahalagang intermediate sa conversion ng carbohydrates at protina sa mga organismo; kinakailangang isaalang-alang ang pagkakaroon ng enol at keto form ng acid.
Ang mga pangunahing pamamaraan para sa pagkuha ng mga carboxylic acid ay: hydrolysis ng kanilang mga derivatives (nitriles, esters, atbp.), Oksihenasyon ng mga alkenes, alcohols at aldehydes, fermentation ng carbohydrates, atbp.
Kontrolin ang mga tanong at pagsasanay:
1. Isulat ang mga pormula sa istruktura ng lahat ng isomeric acid ng komposisyon C 5 H 10 O 2 . Pangalanan ang mga compound ayon sa trivial at substitutional nomenclature. Ihambing ang mga acidic na katangian ng mga isomer.
2. Isulat para sa propionic (propanoic) acid ang mga equation ng mga posibleng reaksyon sa metallic sodium, copper (II) hydroxide, sodium carbonate, ethyl alcohol, ammonia, na sinusundan ng pag-init. Pangalanan ang mga resultang compound ayon sa IUPAC nomenclature.
3. Isulat ang mga istrukturang formula ng isomeric dicarboxylic acid ng komposisyon C 4 H 6 O 4 . Pangalanan ang mga nakuhang isomer.
4. Isulat ang mga istrukturang formula ng isomeric unsaturated acids ng komposisyon C 4 H 6 O 2 . Alin sa kanila ang magkakaroon ng mga geometric na isomer? Pangalanan ang structural at spatial isomers.
5. Isulat ang structural formula ng triglyceride - dipalmitolein. Isulat ang mga equation para sa bromination, saponification na may sodium hydroxide, oxidation na may potassium permanganate ng ipinahiwatig na taba.
6. Ihambing ang mga acidic na katangian ng acetic, oxoacetic, oxalic at hydroxyacetic acids.
MGA HALIMBAWA NG MGA SOLUSYON NG MGA KARANIWANG PROBLEMA
| " |


 >
>