Alam ng sangkatauhan ang ilang uri ng enerhiya - mekanikal na enerhiya (kinetic at potensyal), panloob na enerhiya (thermal), field energy (gravitational, electromagnetic at nuclear), kemikal. Hiwalay, ito ay nagkakahalaga ng pag-highlight ng enerhiya ng pagsabog, ...
Vacuum na enerhiya at umiiral pa rin sa teorya - madilim na enerhiya. Sa artikulong ito, ang una sa seksyong "Heat Engineering", susubukan ko sa isang simple at naa-access na wika gamit praktikal na halimbawa, pag-usapan ang pinakamahalagang anyo ng enerhiya sa buhay ng mga tao - tungkol sa thermal energy at tungkol sa panganganak sa kanya sa oras lakas-thermal.
Ang ilang mga salita upang maunawaan ang lugar ng heat engineering bilang isang sangay ng agham ng pagkuha, paglilipat at paggamit ng thermal energy. Ang modernong heat engineering ay lumitaw mula sa pangkalahatang thermodynamics, na siya namang isa sa mga sangay ng pisika. Ang Thermodynamics ay literal na "mainit" kasama ang "kapangyarihan". Kaya, ang thermodynamics ay ang agham ng "pagbabago sa temperatura" ng isang sistema.
Ang epekto sa system mula sa labas, kung saan nagbabago ang panloob na enerhiya nito, ay maaaring resulta ng paglipat ng init. Thermal na enerhiya, na nakukuha o nawala ng system bilang resulta ng naturang pakikipag-ugnayan sa kapaligiran, ay tinatawag dami ng init at sinusukat sa SI system sa Joules.
Kung ikaw ay hindi isang heat engineer at hindi nakikitungo sa mga isyu sa heat engineering sa araw-araw, kung gayon kapag nakatagpo mo ang mga ito, minsan nang walang karanasan ay maaaring napakahirap na mabilis na malaman ang mga ito. Mahirap isipin kahit na ang mga sukat ng nais na halaga ng dami ng init at init na kapangyarihan nang walang karanasan. Ilang Joules ng enerhiya ang kailangan upang magpainit ng 1000 cubic meters ng hangin mula -37˚С hanggang +18˚С?.. Ano ang kapangyarihan ng pinagmumulan ng init na kailangan upang magawa ito sa loob ng 1 oras? mahirap na mga tanong malayo sa lahat ng mga inhinyero ay nakakasagot ng "right off the bat" ngayon. Minsan naaalala pa nga ng mga eksperto ang mga formula, ngunit iilan lamang ang maaaring magsagawa ng mga ito!
Matapos basahin ang artikulong ito hanggang sa dulo, madali mong malulutas ang mga tunay na gawain sa paggawa at sambahayan na may kaugnayan sa pagpainit at paglamig ng iba't ibang materyales. Ang pag-unawa sa pisikal na kakanyahan ng mga proseso ng paglipat ng init at kaalaman sa mga simpleng pangunahing formula ay ang mga pangunahing bloke sa pundasyon ng kaalaman sa heat engineering!
Ang dami ng init sa iba't ibang pisikal na proseso.
Karamihan sa mga kilalang substance ay maaaring nasa solid, liquid, gas o plasma states sa iba't ibang temperatura at pressure. Transisyon mula sa isang pinagsama-samang estado patungo sa isa pa nagaganap sa pare-parehong temperatura(sa kondisyon na ang presyon at iba pang mga parameter ay hindi nagbabago kapaligiran) at sinamahan ng pagsipsip o pagpapalabas ng thermal energy. Sa kabila ng katotohanan na 99% ng bagay sa Uniberso ay nasa estado ng plasma, hindi namin isasaalang-alang ang estado ng pagsasama-sama sa artikulong ito.
Isaalang-alang ang graph na ipinapakita sa figure. Ipinapakita nito ang pag-asa ng temperatura ng isang sangkap T sa dami ng init Q, summed up sa isang tiyak na saradong sistema na naglalaman ng isang tiyak na masa ng isang partikular na sangkap.

1. Isang solid na may temperatura T1, pinainit sa isang temperatura Tm, paggastos sa prosesong ito ng halaga ng init na katumbas ng Q1 .
2. Susunod, magsisimula ang proseso ng pagkatunaw, na nangyayari sa isang pare-parehong temperatura Tpl(temperatura ng pagkatunaw). Upang matunaw ang buong masa ng isang solid, kinakailangan na gumastos ng thermal energy sa halaga Q2 — Q1 .
3. Susunod, ang likido na nagreresulta mula sa pagkatunaw ng isang solid ay pinainit hanggang sa kumukulo (pagbuo ng gas) Tkp, paggastos sa halagang ito ng init na katumbas ng Q3-Q2 .
4. Ngayon sa patuloy na kumukulo Tkp kumukulo at sumingaw ang likido, nagiging gas. Para sa paglipat ng buong masa ng likido sa gas, kinakailangan na gumastos ng thermal energy sa halaga Q4-Q3.
5. Sa huling hakbang ang gas ay pinainit sa isang temperatura Tkp hanggang sa ilang temperatura T2. Sa kasong ito, ang halaga ng halaga ng init ay magiging Q5-Q4. (Kung painitin natin ang gas sa temperatura ng ionization, ang gas ay magiging plasma.)
Kaya, pinainit ang orihinal solid temperatura T1 hanggang sa temperatura T2 gumastos kami ng thermal energy sa halaga Q5, isinasalin ang substance sa pamamagitan ng tatlong estado ng pagsasama-sama.
Lumipat sa loob magkasalungat na daan, aalisin namin ang parehong dami ng init mula sa sangkap Q5, na dumadaan sa mga yugto ng condensation, crystallization at paglamig mula sa temperatura T2 hanggang sa temperatura T1. Siyempre, isinasaalang-alang namin ang isang saradong sistema na walang pagkawala ng enerhiya sa panlabas na kapaligiran.
Tandaan na ang paglipat mula sa solid state hanggang sa gas na estado ay posible, na lampasan ang likidong bahagi. Ang prosesong ito ay tinatawag na sublimation, at ang reverse na proseso ay tinatawag na desublimation.
Kaya, naunawaan namin na ang mga proseso ng mga paglipat sa pagitan ng mga pinagsama-samang estado ng isang sangkap ay nailalarawan sa pamamagitan ng pagkonsumo ng enerhiya sa isang pare-parehong temperatura. Kapag ang isang sangkap ay pinainit, na nasa isang hindi nagbabagong estado ng pagsasama-sama, ang temperatura ay tumataas at kumonsumo din. thermal energy.
Ang mga pangunahing formula para sa paglipat ng init.
Ang mga formula ay napaka-simple.
Dami ng init Q sa J ay kinakalkula ng mga formula:
1. Mula sa bahagi ng pagkonsumo ng init, ibig sabihin, mula sa bahagi ng pagkarga:
1.1. Kapag pinainit (pinalamig):
Q = m * c *(T2 -T1)
m – masa ng sangkap sa kg
may- tiyak na kapasidad ng init ng isang sangkap sa J / (kg * K)
1.2. Kapag natutunaw (nagyeyelo):
Q = m * λ
λ – tiyak na init ng pagkatunaw at pagkikristal ng isang sangkap sa J/kg
1.3. Sa panahon ng pagkulo, pagsingaw (condensation):
Q = m * r
r – tiyak na init ng gas formation at condensation ng matter sa J/kg
2. Mula sa gilid ng paggawa ng init, iyon ay, mula sa gilid ng pinagmulan:
2.1. Kapag nagsusunog ng gasolina:
Q = m * q
q – tiyak na init ng pagkasunog ng gasolina sa J/kg
2.2. Kapag nagko-convert ng kuryente sa thermal energy (Joule-Lenz law):
Q =t *I *U =t *R *I ^2=(t /r)*U ^2
t – oras sa s
ako – kasalukuyang halaga sa A
U – r.m.s. boltahe sa V
R – paglaban sa pag-load sa ohms
Napagpasyahan namin na ang dami ng init ay direktang proporsyonal sa masa ng sangkap sa lahat ng mga pagbabagong bahagi at, kapag pinainit, ay direktang proporsyonal sa pagkakaiba ng temperatura. Mga koepisyent ng proporsyonalidad ( c , λ , r , q ) para sa bawat sangkap ay may sariling mga halaga at tinutukoy ng empirically (kinuha mula sa mga sangguniang libro).
Lakas-thermal N sa W ay ang dami ng init na inilipat sa system sa isang tiyak na oras:
N=Q/t
Ang mas mabilis na gusto nating painitin ang katawan sa isang tiyak na temperatura, mas malaki ang kapangyarihan ay dapat na pinagmumulan ng thermal energy - lahat ay lohikal.
Pagkalkula sa Excel na inilapat na gawain.
Sa buhay, madalas na kinakailangan na gumawa ng mabilis na tinantyang pagkalkula upang maunawaan kung makatuwirang ipagpatuloy ang pag-aaral ng isang paksa, paggawa ng isang proyekto at detalyadong tumpak na mga kalkulasyon na masinsinang paggawa. Sa pamamagitan ng paggawa ng kalkulasyon sa loob ng ilang minuto kahit na may katumpakan na ± 30%, makakagawa ka ng mahalagang desisyon sa pamamahala na magiging 100 beses na mas mura at 1000 beses na mas mabilis at, bilang resulta, 100,000 beses na mas mahusay kaysa sa pagsasagawa ng tumpak na pagkalkula sa loob ng isang linggo, kung hindi man at isang buwan, ng isang grupo ng mga mamahaling espesyalista ...
Mga kondisyon ng problema:
Sa lugar ng tindahan para sa paghahanda ng pinagsamang metal na may sukat na 24m x 15m x 7m, nag-import kami ng pinagsamang metal mula sa isang bodega sa kalye sa halagang 3 tonelada. Ang pinagsamang metal ay may yelo na may kabuuang masa na 20 kg. Sa labas -37˚С. Anong dami ng init ang kailangan upang mapainit ang metal sa + 18˚С; init ang yelo, tunawin ito at painitin ang tubig hanggang +18˚С; init ang buong dami ng hangin sa silid, sa pag-aakala na ang pag-init ay ganap na pinatay bago iyon? Anong kapangyarihan ang dapat magkaroon ng sistema ng pag-init kung ang lahat ng nasa itaas ay dapat makumpleto sa loob ng 1 oras? (Napakabagsik at halos hindi makatotohanang mga kondisyon - lalo na tungkol sa hangin!)
Gagawin namin ang pagkalkula sa programaMS Excel o sa programaOo Calc.
Para sa pag-format ng kulay ng mga cell at font, tingnan ang pahina ng "".
Paunang data:
1. Isinulat namin ang mga pangalan ng mga sangkap:
sa cell D3: bakal
sa cell E3: yelo
sa cell F3: yelo/tubig
sa cell G3: Tubig
sa cell G3: Hangin
2. Ipinasok namin ang mga pangalan ng mga proseso:
sa mga cell D4, E4, G4, G4: init
sa cell F4: natutunaw
3. Tiyak na kapasidad ng init ng mga sangkap c sa J / (kg * K) sumulat kami para sa bakal, yelo, tubig at hangin, ayon sa pagkakabanggit
sa cell D5: 460
sa cell E5: 2110
sa cell G5: 4190
sa cell H5: 1005
4. tiyak na init natutunaw na yelo λ sa J/kg ipasok
sa cell F6: 330000
5. Masa ng mga sangkap m sa kg pumapasok kami, ayon sa pagkakabanggit, para sa bakal at yelo
sa cell D7: 3000
sa cell E7: 20
Dahil ang masa ay hindi nagbabago kapag ang yelo ay nagiging tubig,
sa mga cell F7 at G7: =E7 =20
Ang masa ng hangin ay matatagpuan sa pamamagitan ng pagpaparami ng dami ng silid sa pamamagitan ng tiyak na gravity
sa cell H7: =24*15*7*1.23 =3100
6. Oras ng proseso t sa ilang minuto, minsan lang kaming sumulat para sa bakal
sa cell D8: 60
Ang mga halaga ng oras para sa pagpainit ng yelo, pagkatunaw nito at pag-init ng nagresultang tubig ay kinakalkula mula sa kondisyon na ang lahat ng tatlong prosesong ito ay dapat buuin sa parehong oras ng oras na inilaan para sa pagpainit ng metal. Binabasa namin nang naaayon
sa cell E8: =E12/(($E$12+$F$12+$G$12)/D8) =9,7
sa cell F8: =F12/(($E$12+$F$12+$G$12)/D8) =41,0
sa cell G8: =G12/(($E$12+$F$12+$G$12)/D8) =9,4
Ang hangin ay dapat ding magpainit sa parehong inilaang oras, mababasa natin
sa cell H8: =D8 =60,0
7. Ang paunang temperatura ng lahat ng mga sangkap T1 sa ˚C kami pumasok
sa cell D9: -37
sa cell E9: -37
sa cell F9: 0
sa cell G9: 0
sa cell H9: -37
8. Panghuling temperatura ng lahat ng mga sangkap T2 sa ˚C kami pumasok
sa cell D10: 18
sa cell E10: 0
sa cell F10: 0
sa cell G10: 18
sa cell H10: 18
Sa tingin ko ay hindi dapat magkaroon ng anumang mga katanungan sa mga aytem 7 at 8.

Mga resulta ng pagkalkula:
9. Dami ng init Q sa KJ na kinakailangan para sa bawat proseso na aming kinakalkula
para sa steel heating sa cell D12: =D7*D5*(D10-D9)/1000 =75900
para sa pagpainit ng yelo sa cell E12: =E7*E5*(E10-E9)/1000 = 1561
para sa pagtunaw ng yelo sa cell F12: =F7*F6/1000 = 6600
para sa pagpainit ng tubig sa cell G12: =G7*G5*(G10-G9)/1000 = 1508
para sa pagpainit ng hangin sa cell H12: =H7*H5*(H10-H9)/1000 = 171330
Ang kabuuang halaga ng thermal energy na kinakailangan para sa lahat ng mga proseso ay binabasa
sa pinagsamang cell D13E13F13G13H13: =SUM(D12:H12) = 256900
Sa mga cell D14, E14, F14, G14, H14, at ang pinagsamang cell D15E15F15G15H15, ang dami ng init ay ibinibigay sa isang arc unit ng pagsukat - sa Gcal (sa gigacalories).
10. Lakas-thermal N sa kW, kinakailangan para sa bawat isa sa mga proseso ay kinakalkula
para sa steel heating sa cell D16: =D12/(D8*60) =21,083
para sa pagpainit ng yelo sa cell E16: =E12/(E8*60) = 2,686
para sa pagtunaw ng yelo sa cell F16: =F12/(F8*60) = 2,686
para sa pagpainit ng tubig sa cell G16: =G12/(G8*60) = 2,686
para sa pagpainit ng hangin sa cell H16: =H12/(H8*60) = 47,592
Ang kabuuang thermal power na kinakailangan upang maisagawa ang lahat ng mga proseso sa isang pagkakataon t kalkulado
sa pinagsamang cell D17E17F17G17H17: =D13/(D8*60) = 71,361
Sa mga cell D18, E18, F18, G18, H18, at ang pinagsamang cell D19E19F19G19H19, ang thermal power ay ibinibigay sa isang arc unit ng pagsukat - sa Gcal / h.
Kinukumpleto nito ang pagkalkula sa Excel.
Natuklasan:
Tandaan na nangangailangan ng higit sa dalawang beses na mas maraming enerhiya upang magpainit ng hangin kaysa sa pag-init ng parehong masa ng bakal.
Kapag nag-iinit ng tubig, ang mga gastos sa enerhiya ay dalawang beses na mas malaki kaysa kapag nagpainit ng yelo. Ang proseso ng pagtunaw ay kumonsumo ng maraming beses na mas maraming enerhiya kaysa sa proseso ng pag-init (na may maliit na pagkakaiba sa temperatura).
Ang pag-init ng tubig ay kumokonsumo ng sampung beses na mas maraming init kaysa sa pag-init ng bakal at apat na beses na higit pa kaysa sa pag-init ng hangin.
Para sa tumatanggap impormasyon tungkol sa pagpapalabas ng mga bagong artikulo at para sa pag-download ng mga gumaganang file ng program Hinihiling ko sa iyo na mag-subscribe sa mga anunsyo sa window na matatagpuan sa dulo ng artikulo o sa window sa tuktok ng pahina.
Matapos ipasok ang iyong address Email at pag-click sa pindutang "Tumanggap ng mga anunsyo ng mga artikulo" HUWAG KALIMUTANKUMPIRMAHIN SUBSCRIPTION sa pamamagitan ng pag-click sa link sa isang liham na agad na darating sa iyo sa tinukoy na mail (minsan - sa folder « Spam » )!
Naalala namin ang mga konsepto ng "dami ng init" at "thermal power", isinasaalang-alang ang mga pangunahing formula para sa paglipat ng init, at sinuri ang isang praktikal na halimbawa. Sana ay simple, naiintindihan at kawili-wili ang aking wika.
Inaasahan ko ang mga tanong at komento sa artikulo!
magtanong PAGGALANG file ng pag-download ng gawa ng may-akda PAGKATAPOS MAGSUBSCRIPTION para sa mga anunsyo ng artikulo.
730. Bakit ginagamit ang tubig upang palamig ang ilang mekanismo?
Mahusay ang tubig tiyak na init, na nag-aambag sa mahusay na pag-aalis ng init mula sa mekanismo.
731. Sa anong kaso dapat gumamit ng mas maraming enerhiya: para sa pagpainit ng isang litro ng tubig ng 1 °C o para sa pagpainit ng isang daang gramo ng tubig ng 1 °C?
Upang magpainit ng isang litro ng tubig, dahil mas malaki ang masa, mas maraming enerhiya ang kailangang gastusin.
732. Ang mga cupronickel at pilak na tinidor ng parehong masa ay inilubog sa mainit na tubig. Pareho ba silang natatanggap ng init mula sa tubig?
Ang isang cupronickel fork ay makakatanggap ng higit na init, dahil ang tiyak na init ng cupronickel ay mas malaki kaysa sa pilak.
733. Ang isang piraso ng tingga at isang piraso ng cast iron ng parehong masa ay hinampas ng tatlong beses ng isang sledgehammer. Aling bahagi ang naging mas mainit?
Mas mag-iinit ang tingga dahil ang tiyak na kapasidad ng init nito ay mas mababa kaysa sa cast iron, at mas kaunting enerhiya ang kailangan upang mapainit ang tingga.
734. Ang isang prasko ay naglalaman ng tubig, ang isa naman ay naglalaman ng kerosene ng parehong masa at temperatura. Ang isang pantay na pinainit na bakal na kubo ay itinapon sa bawat prasko. Ano ang magpapainit sa mas mataas na temperatura - tubig o kerosene?
Kerosene.
735. Bakit hindi gaanong matalas ang pagbabagu-bago ng temperatura sa taglamig at tag-araw sa mga lungsod sa dalampasigan kaysa sa mga lungsod na nasa loob ng bansa?
Ang tubig ay umiinit at lumalamig nang mas mabagal kaysa sa hangin. Sa taglamig, lumalamig ito at nagpapagalaw ng mainit na hangin sa lupa, na ginagawang mas mainit ang klima sa baybayin.
736. Ang tiyak na kapasidad ng init ng aluminyo ay 920 J/kg °C. Anong ibig sabihin nito?
Nangangahulugan ito na nangangailangan ng 920 J upang mapainit ang 1 kg ng aluminyo sa pamamagitan ng 1 °C.
737. Ang mga aluminyo at tansong bar na may parehong masa na 1 kg ay pinalamig ng 1 °C. Magkano ang magbabago ng panloob na enerhiya ng bawat bloke? Aling bar ang mas magbabago at kung magkano?
738. Anong halaga ng init ang kailangan upang mapainit ang isang kilo na iron billet ng 45 °C?

739. Gaano karaming init ang kinakailangan upang magpainit ng 0.25 kg ng tubig mula 30°C hanggang 50°C?

740. Paano magbabago ang panloob na enerhiya ng dalawang litro ng tubig kapag pinainit ng 5 °C?

741. Gaano karaming init ang kailangan para magpainit ng 5 g ng tubig mula 20 °C hanggang 30 °C?

742. Anong dami ng init ang kailangan para magpainit ng aluminum ball na tumitimbang ng 0.03 kg ng 72 °C?

743. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 15 kg ng tanso ng 80 °C.

744. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 5 kg ng tanso mula 10 °C hanggang 200 °C.

745. Anong dami ng init ang kailangan para magpainit ng 0.2 kg ng tubig mula 15 °C hanggang 20 °C?

746. Ang tubig na tumitimbang ng 0.3 kg ay lumamig ng 20 °C. Gaano nababawasan ang panloob na enerhiya ng tubig?

747. Gaano karaming init ang kailangan para magpainit ng 0.4 kg ng tubig sa temperaturang 20 °C hanggang sa temperaturang 30 °C?

748. Magkano ang init na ginugol sa pagpainit ng 2.5 kg ng tubig sa pamamagitan ng 20 °C?

749. Gaano karaming init ang pinakawalan nang ang 250 g ng tubig ay lumamig mula 90 °C hanggang 40 °C?

750. Anong halaga ng init ang kinakailangan upang magpainit ng 0.015 litro ng tubig ng 1 °C?

751. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng isang lawa na may volume na 300 m3 ng 10 °C?

752. Gaano karaming init ang dapat ibigay sa 1 kg ng tubig upang mapataas ang temperatura nito mula 30°C hanggang 40°C?

753. Ang tubig na may dami na 10 litro ay lumamig mula sa temperaturang 100 °C hanggang sa temperaturang 40 °C. Gaano karaming init ang inilabas sa kasong ito?

754. Kalkulahin ang dami ng init na kinakailangan upang magpainit ng 1 m3 ng buhangin sa pamamagitan ng 60 °C.

755. Dami ng hangin 60 m3, tiyak na kapasidad ng init 1000 J/kg °C, air density 1.29 kg/m3. Gaano karaming init ang kailangan upang itaas ito sa 22°C?

756. Ang tubig ay pinainit ng 10 ° C, na gumagastos ng 4.20 103 J ng init. Tukuyin ang dami ng tubig.
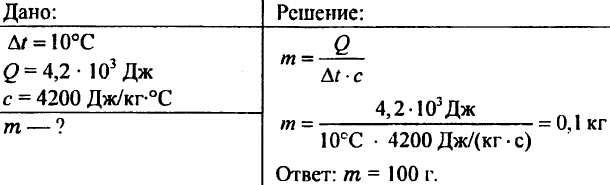
757. Ang tubig na tumitimbang ng 0.5 kg ay nag-ulat ng 20.95 kJ ng init. Ano ang temperatura ng tubig kung ang unang temperatura ng tubig ay 20°C?
758. 8 kg ng tubig sa 10 °C ay ibinuhos sa isang tansong kasirola na tumitimbang ng 2.5 kg. Gaano karaming init ang kailangan para kumulo ang tubig sa isang kasirola?

759. Ang isang litro ng tubig sa temperatura na 15 °C ay ibinubuhos sa isang tansong sandok na tumitimbang ng 300 g. Gaano karaming init ang kailangan upang mapainit ang tubig sa sandok ng 85 °C?

760. Ang isang piraso ng heated granite na tumitimbang ng 3 kg ay inilalagay sa tubig. Ang Granite ay naglilipat ng 12.6 kJ ng init sa tubig, na lumalamig ng 10 °C. Ano ang tiyak na kapasidad ng init ng bato?

761. Ang mainit na tubig sa 50°C ay idinagdag sa 5 kg ng tubig sa 12°C, na nakakuha ng pinaghalong may temperaturang 30°C. Gaano karaming tubig ang naidagdag?

762. Ang tubig sa 20°C ay idinagdag sa 3 litro ng tubig sa 60°C upang makakuha ng tubig sa 40°C. Gaano karaming tubig ang naidagdag?

763. Ano ang magiging temperatura ng pinaghalong kung ang 600 g ng tubig sa 80 °C ay ihalo sa 200 g ng tubig sa 20 °C?

764. Isang litro ng tubig sa 90°C ang ibinuhos sa tubig sa 10°C, at ang temperatura ng tubig ay naging 60°C. Gaano karaming malamig na tubig ang naroon?

765. Tukuyin kung gaano karaming mainit na tubig na pinainit hanggang 60°C ang dapat ibuhos sa isang sisidlan kung ang sisidlan ay naglalaman na ng 20 litro ng malamig na tubig sa temperatura na 15°C; ang temperatura ng pinaghalong ay dapat na 40 °C.

766. Tukuyin kung gaano karaming init ang kinakailangan upang magpainit ng 425 g ng tubig sa pamamagitan ng 20 °C.

767. Ilang degrees ang iinit ng 5 kg ng tubig kung ang tubig ay tumatanggap ng 167.2 kJ?

768. Gaano karaming init ang kinakailangan upang magpainit ng m gramo ng tubig sa temperaturang t1 hanggang sa temperaturang t2?
769. Ang 2 kg ng tubig ay ibinubuhos sa isang calorimeter sa temperatura na 15 °C. Sa anong temperatura magpapainit ang tubig ng calorimeter kung ang isang tansong timbang na 500 g na pinainit hanggang 100 °C ay ibababa dito? Ang tiyak na kapasidad ng init ng tanso ay 0.37 kJ/(kg °C).

770. May mga piraso ng tanso, lata at aluminyo ng parehong dami. Alin sa mga pirasong ito ang may pinakamalaki at alin ang pinakamaliit na kapasidad ng init?

771. 450 g ng tubig, ang temperatura kung saan ay 20 °C, ay ibinuhos sa calorimeter. Kapag ang 200 g ng iron filings na pinainit hanggang 100°C ay inilubog sa tubig na ito, ang temperatura ng tubig ay naging 24°C. Tukuyin ang tiyak na kapasidad ng init ng sawdust.

772. Ang isang tansong calorimeter na tumitimbang ng 100 g ay naglalaman ng 738 g ng tubig, na ang temperatura ay 15 °C. Ang 200 g ng tanso ay ibinaba sa calorimeter na ito sa temperatura na 100 °C, pagkatapos nito ang temperatura ng calorimeter ay tumaas sa 17 °C. Ano ang tiyak na kapasidad ng init ng tanso?

773. Ang isang bolang bakal na tumitimbang ng 10 g ay inilabas mula sa hurno at ibinaba sa tubig sa temperatura na 10 °C. Ang temperatura ng tubig ay tumaas hanggang 25°C. Ano ang temperatura ng bola sa oven kung ang masa ng tubig ay 50 g? Ang tiyak na kapasidad ng init ng bakal ay 0.5 kJ/(kg °C).
776. Ang tubig na tumitimbang ng 0.95 g sa temperatura na 80 °C ay hinaluan ng tubig na tumitimbang ng 0.15 g sa temperatura na 15 °C. Tukuyin ang temperatura ng pinaghalong. 779. Ang isang bakal na pait na tumitimbang ng 2 kg ay pinainit sa temperatura na 800 °C at pagkatapos ay ibinaba sa isang sisidlan na naglalaman ng 15 litro ng tubig sa temperatura na 10 °C. Sa anong temperatura papainitin ang tubig sa sisidlan?

(Indikasyon. Upang malutas ang problemang ito, kinakailangan na lumikha ng isang equation kung saan ang nais na temperatura ng tubig sa sisidlan pagkatapos ibaba ang cutter ay kinuha bilang hindi alam.)
780. Anong temperatura ang makukuha ng tubig kung paghaluin mo ang 0.02 kg ng tubig sa 15 °C, 0.03 kg ng tubig sa 25 °C, at 0.01 kg ng tubig sa 60 °C?

781. Ang pag-init ng isang well-ventilated na klase ay nangangailangan ng halaga ng init na 4.19 MJ bawat oras. Ang tubig ay pumapasok sa mga heating radiator sa 80°C at lumalabas sa 72°C. Gaano karaming tubig ang dapat ibigay sa mga radiator bawat oras?

782. Ang tingga na tumitimbang ng 0.1 kg sa temperatura na 100 °C ay inilubog sa isang aluminum calorimeter na tumitimbang ng 0.04 kg na naglalaman ng 0.24 kg ng tubig sa temperatura na 15 °C. Pagkatapos nito, ang temperatura ng 16 °C ay itinatag sa calorimeter. Ano ang tiyak na kapasidad ng init ng tingga?

(o paglipat ng init).
Tiyak na kapasidad ng init ng isang sangkap.
Kapasidad ng init ay ang dami ng init na hinihigop ng katawan kapag pinainit ng 1 degree.
Ang kapasidad ng init ng katawan ay ipinahiwatig ng malaking titik na Latin Sa.
Ano ang tumutukoy sa kapasidad ng init ng isang katawan? Una sa lahat, mula sa masa nito. Malinaw na ang pag-init, halimbawa, ang 1 kilo ng tubig ay mangangailangan ng higit na init kaysa sa pagpainit ng 200 gramo.
Paano ang tungkol sa uri ng sangkap? Gumawa tayo ng isang eksperimento. Kumuha tayo ng dalawang magkatulad na sisidlan at, pagbuhos ng tubig na tumitimbang ng 400 g sa isa sa mga ito, at langis ng gulay na tumitimbang ng 400 g sa isa pa, sisimulan nating painitin ang mga ito sa tulong ng magkaparehong mga burner. Sa pamamagitan ng pagmamasid sa mga pagbasa ng mga thermometer, makikita natin na mabilis uminit ang langis. Upang magpainit ng tubig at langis sa parehong temperatura, ang tubig ay dapat na pinainit nang mas matagal. Ngunit habang pinainit natin ang tubig, mas maraming init ang natatanggap nito mula sa burner.
Kaya, upang mapainit ang parehong masa ng iba't ibang mga sangkap sa parehong temperatura, iba't ibang halaga ng init ang kinakailangan. Ang dami ng init na kinakailangan upang magpainit ng isang katawan at, dahil dito, ang kapasidad ng init nito ay nakasalalay sa uri ng sangkap kung saan binubuo ang katawan na ito.
Kaya, halimbawa, upang mapataas ang temperatura ng tubig na may mass na 1 kg sa pamamagitan ng 1 ° C, isang halaga ng init na katumbas ng 4200 J ay kinakailangan, at upang painitin ang parehong masa ng langis ng mirasol ng 1 ° C, isang halaga ng kailangan ang init na katumbas ng 1700 J.
Ang pisikal na dami na nagpapakita kung gaano karaming init ang kinakailangan upang magpainit ng 1 kg ng isang sangkap sa pamamagitan ng 1 ºС ay tinatawag tiyak na init sangkap na ito.
Ang bawat sangkap ay may sariling tiyak na kapasidad ng init, na tinutukoy ng Latin na titik c at sinusukat sa joules bawat kilo-degree (J / (kg ° C)).
Ang tiyak na kapasidad ng init ng parehong sangkap sa iba't ibang estado ng pagsasama-sama(solid, liquid at gaseous) ay iba. Halimbawa, ang tiyak na kapasidad ng init ng tubig ay 4200 J/(kg ºС), at ang tiyak na kapasidad ng init ng yelo ay 2100 J/(kg ºС); Ang aluminyo sa solid state ay may tiyak na kapasidad ng init na 920 J/(kg - °C), at sa likidong estado ito ay 1080 J/(kg - °C).
Tandaan na ang tubig ay may napakataas na tiyak na kapasidad ng init. Samakatuwid, ang tubig sa mga dagat at karagatan, na umiinit sa tag-araw, ay sumisipsip ng malaking halaga ng init mula sa hangin. Dahil dito, sa mga lugar na iyon na matatagpuan malapit sa malalaking anyong tubig, ang tag-araw ay hindi kasing init sa mga lugar na malayo sa tubig.
Pagkalkula ng dami ng init na kinakailangan upang mapainit ang katawan o inilabas nito sa panahon ng paglamig.
Mula sa nabanggit, malinaw na ang dami ng init na kinakailangan upang magpainit ng katawan ay nakasalalay sa uri ng sangkap kung saan binubuo ang katawan (i.e., ang tiyak na kapasidad ng init nito) at sa masa ng katawan. Malinaw din na ang dami ng init ay nakadepende sa kung gaano karaming degree ang tataas natin sa temperatura ng katawan.
Kaya, upang matukoy ang dami ng init na kinakailangan upang mapainit ang katawan o ilalabas nito sa panahon ng paglamig, kailangan mong i-multiply ang tiyak na init ng katawan sa pamamagitan ng masa nito at sa pagkakaiba sa pagitan ng pangwakas at paunang temperatura nito:
Q = cm (t 2 - t 1 ) ,
saan Q- dami ng init, c ay ang tiyak na kapasidad ng init, m- bigat ng katawan, t 1 - paunang temperatura, t 2 ay ang huling temperatura.
Kapag naiinitan ang katawan t 2 > t 1 at samakatuwid Q > 0 . Kapag pinalamig ang katawan t 2at< t 1 at samakatuwid Q< 0 .
Kung alam ang kapasidad ng init ng buong katawan Sa, Q ay tinutukoy ng formula:
Q \u003d C (t 2 - t 1 ) .
Sa pamamagitan ng kahulugan, ang isang calorie ay ang dami ng init na kinakailangan upang mapainit ang isa kubiko sentimetro tubig sa pamamagitan ng 1 degree Celsius. Ang isang gigacalorie, na ginagamit upang sukatin ang thermal energy sa thermal power engineering at mga utility, ay isang bilyong calories. Mayroong 100 sentimetro sa 1 metro, kaya mayroong 100 x 100 x 100 = 1,000,000 sentimetro sa isang metro kubiko. Kaya, upang magpainit ng isang kubo ng tubig sa pamamagitan ng
1 degree, aabutin ito ng isang milyong calories o 0.001 Gcal.
Sa aking lungsod, ang presyo ng pagpainit ay 1132.22 rubles / Gcal, at ang presyo ng mainit na tubig ay 71.65 rubles / m3, ang presyo ng malamig na tubig ay 16.77 rubles / m3.
Magkano Gcal ang ginagastos para magpainit ng 1 cubic meter ng tubig?
Sa tingin ko
s x 1132.22 \u003d 71.65 - 16.77 at sa ganitong paraan nalulutas ko ang mga equation upang malaman kung ano ang katumbas ng s (Gcal), iyon ay, ito ay katumbas ng 0.0484711452 Gcal
May duda ako, sa palagay ko, mali ang desisyon ko
SAGOT:
Wala akong mahanap na anumang mga error sa iyong pagkalkula.
Naturally, ang halaga ng wastewater (water disposal) ay hindi dapat isama sa mga ibinigay na taripa.
Ang isang tinatayang pagkalkula para sa lungsod ng Izhevsk ayon sa mga lumang pamantayan ay ganito ang hitsura:
0.19 Gcal bawat tao bawat buwan (nakansela na ang pamantayang ito, ngunit wala nang iba, halimbawa ay gagawin nito) / 3.6 cubic meters. bawat tao bawat buwan (rate ng pagkonsumo ng mainit na tubig) = 0.05278 Gcal bawat 1 metro kubiko. (napakaraming init ang kailangan para magpainit ng 1 metro kubiko ng malamig na tubig sa karaniwang temperatura ng mainit na tubig, na, ipaalala ko sa iyo, ay 60 degrees C).
Para sa isang mas tumpak na pagkalkula ng dami ng thermal energy para sa pagpainit ng tubig sa pamamagitan ng direktang paraan batay sa mga pisikal na dami (at hindi ang reverse na paraan batay sa mga naaprubahang taripa para sa supply ng mainit na tubig) - Inirerekomenda ko ang paggamit template ng pagkalkula ng taripa ng mainit na tubig (REC UR). Ang formula ng pagkalkula, bukod sa iba pang mga bagay, ay gumagamit ng temperatura ng malamig na tubig sa tag-araw at taglamig (pag-init), ang tagal ng mga panahong ito.
Mga Tag: gigacalorie, mainit na tubig
- Nagbabayad kami para sa mga serbisyo ng mainit na tubig, ang temperatura ay mas mababa kaysa sa pamantayan. Anong gagawin?
- Ang pagpapatuloy ng panahon ng pagdiskonekta ng DHW na itinatag ng Mga Panuntunan ay hindi ilegal - desisyon ng Korte Suprema ng Russian Federation (2017)
- Fairer Tariff Initiative at Hot Water Metering Methodology
- Sa pamamaraan para sa muling pagkalkula ng halaga ng pagbabayad para sa pagpainit at mainit na supply ng tubig sa panahon ng mga shutdown - paglilinaw ng Rospotrebnadzor para sa SD
- Sa accounting para sa heat carrier sa isang closed heat supply system - sulat ng Ministry of Construction ng Russian Federation noong Marso 31, 2015 No. 9116-OD / 04
- UR - Sa pagbabawas ng pagbabayad para sa pagpainit at supply ng mainit na tubig - sulat mula sa Ministry of Energy ng UR ng 17.08.2015 No. 11-10 / 5661
- Ano ang karaniwang panahon para sa pagsuri sa isang karaniwang pampainit ng bahay at aparato sa pagsukat ng mainit na tubig?
- Maruming mainit na tubig mula sa gripo. Saan mag-apply?
- Maaari bang umikot ang metro ng tubig sa apartment para sa buong pasukan? Paano magbayad? Mga pahiwatig para sa buwan - 42 metro kubiko
- Ang pamamaraan para sa pagpapanatili ng hiwalay na accounting ng mga gastos sa larangan ng supply ng tubig at kalinisan - order ng Ministry of Construction ng Russian Federation na may petsang Enero 25, 2014 No. 22 / pr
- pagbabayad para sa tubig at kuryente sa isang apartment na walang tirahan
- pagkalkula ng init ayon sa ODPU para sa 1/12
- Power supply
- Malaking bayad para sa isang kuwarto sa isang hostel (17.3 sq.m.)
| Mga komento: (11) | |
| Hint: Ibahagi ang link sa social media kung gusto mo ng higit pang mga tugon/komento! | |
“...- Ilang parrot ang kasya sa iyo, ganyan ang height mo.
- Kailangan talaga! Hindi ako lulunok ng napakaraming loro!…”
Mula sa m / f "38 parrots"
Alinsunod sa mga tuntunin ng internasyonal na SI (International System of Units), ang dami ng thermal energy o ang dami ng init ay sinusukat sa Joules [J], mayroon ding maraming unit ng kiloJoule [kJ] = 1000 J., MegaJoule [MJ] = 1,000,000 J, GigaJoule [ GJ] \u003d 1,000,000,000 J., atbp. Ang yunit na ito ng pagsukat ng thermal energy ang pangunahing internasyonal na yunit at pinakamadalas na ginagamit sa mga kalkulasyon na pang-agham at pang-agham-teknikal.
Gayunpaman, alam nating lahat o kahit minsan ay narinig ang isa pang yunit para sa pagsukat ng dami ng init (o init lang) ay isang calorie, pati na rin ang isang kilocalorie, Megacalorie at Gigacalorie, na nangangahulugang ang mga prefix na kilo, Giga at Mega, tingnan ang halimbawa sa Joules sa itaas. Sa ating bansa, ito ay binuo sa kasaysayan upang kapag kinakalkula ang mga taripa para sa pagpainit, kung ito ay pagpainit gamit ang mga boiler ng kuryente, gas o pellet, kaugalian na isaalang-alang ang halaga ng eksaktong isang Gigacalorie ng thermal energy.
Kaya ano ang Gigacalorie, kilowatt, kilowatt * hour o kilowatt / hour at Joules at paano ito nauugnay?, matututuhan mo sa artikulong ito.
Kaya, ang pangunahing yunit ng thermal energy ay, tulad ng nabanggit na, ang Joule. Ngunit bago pag-usapan ang tungkol sa mga yunit ng pagsukat, kinakailangan, sa prinsipyo, upang ipaliwanag sa antas ng sambahayan kung ano ang thermal energy at kung paano at bakit ito sukatin.
Alam nating lahat mula pagkabata na upang magpainit (makakuha ng thermal energy) kailangan mong magsunog ng isang bagay, kaya lahat tayo ay nagsindi ng apoy, ang tradisyonal na panggatong para sa apoy ay kahoy na panggatong. Kaya, malinaw naman, sa panahon ng pagkasunog ng gasolina (anuman: kahoy na panggatong, karbon, pellets, natural gas, diesel fuel), ang thermal energy (init) ay inilabas. Ngunit para magpainit, halimbawa, iba't ibang dami ng tubig, kailangan ng ibang dami ng panggatong (o iba pang panggatong). Malinaw na ang ilang apoy sa isang apoy ay sapat na upang magpainit ng dalawang litro ng tubig, at upang magluto ng kalahating balde ng sopas para sa buong kampo, kailangan mong mag-imbak ng ilang mga bundle ng kahoy na panggatong. Upang hindi masukat ang mga mahigpit na teknikal na dami tulad ng dami ng init at init ng pagkasunog ng gasolina na may mga bundle ng kahoy na panggatong at mga balde ng sopas, nagpasya ang mga heat engineer na magdala ng kalinawan at kaayusan at sumang-ayon na mag-imbento ng isang yunit para sa dami ng init. Upang maging pareho ang yunit na ito sa lahat ng dako, tinukoy ito bilang mga sumusunod: nangangailangan ng 4,190 calories, o 4.19 kilocalories, upang magpainit ng isang kilo ng tubig ng isang degree sa ilalim ng normal na mga kondisyon (atmospheric pressure), samakatuwid, upang magpainit ng isang gramo ng tubig, isang libong beses na mas kaunting init ay magiging sapat - 4.19 calories.
Ang calorie ay nauugnay sa internasyonal na yunit ng thermal energy, ang Joule, tulad ng sumusunod:
1 calorie = 4.19 Joules.
Kaya, kailangan ng 4.19 Joules ng thermal energy upang magpainit ng 1 gramo ng tubig sa pamamagitan ng isang degree, at 4,190 Joules ng init upang magpainit ng isang kilo ng tubig.
Sa teknolohiya, kasama ang yunit ng pagsukat ng thermal (at anumang iba pang) enerhiya, mayroong isang yunit ng kapangyarihan at, alinsunod sa internasyonal na sistema(SI) ay Watt. Ang konsepto ng kapangyarihan ay naaangkop din sa mga kagamitan sa pag-init. Kung ang isang heating device ay may kakayahang maghatid ng 1 Joule ng thermal energy sa 1 segundo, ang kapangyarihan nito ay 1 watt. Ang kapangyarihan ay ang kakayahan ng isang aparato na gumawa (lumikha) ng isang tiyak na halaga ng enerhiya (sa aming kaso, thermal energy) bawat yunit ng oras. Pagbabalik sa ating halimbawa sa tubig, upang magpainit ng isang kilo (o isang litro, sa kaso ng tubig, ang isang kilo ay katumbas ng isang litro) ng tubig sa pamamagitan ng isang degree Celsius (o Kelvin, anuman), kailangan natin ng lakas na 1 kilocalorie o 4,190 J. ng thermal energy. Upang magpainit ng isang kilo ng tubig sa 1 segundo ng oras sa pamamagitan ng 1 degree, kailangan namin ng device na may sumusunod na kapangyarihan:
4190 J./1 s. = 4 190 W. o 4.19 kW.
Kung gusto nating painitin ang ating kilo ng tubig ng 25 degrees sa parehong segundo, kailangan natin ng dalawampu't limang beses na mas maraming kapangyarihan, i.e.
4.19 * 25 \u003d 104.75 kW.
Kaya, maaari nating tapusin na ang isang pellet boiler na may kapasidad na 104.75 kW. nagpapainit ng 1 litro ng tubig ng 25 degrees sa isang segundo.
Dahil nakarating na tayo sa Watts at kilowatts, dapat din tayong maglagay ng salita tungkol sa kanila. Tulad ng nabanggit na, ang watt ay isang yunit ng kapangyarihan, kabilang ang thermal power ng isang boiler, ngunit bilang karagdagan sa mga pellet boiler at gas boiler, ang mga electric boiler ay pamilyar din sa sangkatauhan, ang kapangyarihan nito ay sinusukat, siyempre, sa parehong kilowatts at hindi sila kumonsumo ng mga pellets o gas, at kuryente, na ang dami nito ay sinusukat sa kilowatt na oras. Ang tamang spelling ng yunit ng enerhiya ay kilowatt * hour (ibig sabihin, kilowatt na pinarami ng isang oras, hindi hinati), ang pagsulat ng kW / oras ay isang pagkakamali!
Sa mga electric boiler, ang elektrikal na enerhiya ay na-convert sa thermal energy (ang tinatawag na Joule heat), at kung ang boiler ay kumonsumo ng 1 kWh ng kuryente, gaano karaming init ang nabuo nito? Upang masagot ang simpleng tanong na ito, kailangan mong magsagawa ng isang simpleng pagkalkula.
Pag-convert ng kilowatts sa kilojoules/segundo (kilojoules bawat segundo) at oras sa segundo: mayroong 3,600 segundo sa isang oras, nakukuha natin ang:
1 kW*h =[ 1 kJ/s]*3600 s.=1,000 J *3600 s = 3,600,000 Joules o 3.6 MJ.
Kaya,
1 kWh = 3.6 MJ.
Sa turn, 3.6 MJ / 4.19 \u003d 0.859 Mcal \u003d 859 kcal \u003d 859,000 cal. Enerhiya (thermal).
Ngayon ay lumipat tayo sa Gigacalorie, ang presyo nito iba't ibang uri ang mga inhinyero sa pag-init ay gustong magbilang ng mga gatong.
1 Gcal = 1,000,000,000 cal.
1,000,000,000 cal. \u003d 4.19 * 1,000,000,000 \u003d 4,190,000,000 J. \u003d 4,190 MJ. = 4.19 GJ.
O, sa pag-alam na 1 kWh = 3.6 MJ, muling kinakalkula namin ang 1 Gigacalorie bawat kilowatt*hour:
1 Gcal = 4190 MJ/3.6 MJ = 1163 kWh!
Kung, pagkatapos basahin ang artikulong ito, nagpasya kang kumunsulta sa isang espesyalista ng aming kumpanya sa anumang isyu na may kaugnayan sa supply ng init, kung gayon ikaw Dito!
Pinagmulan: heat-en.ru