Valența carbonului este ... (număr). Prin urmare, atunci când scrieți formule structurale, patru linii ar trebui să se îndepărteze de carbon, ilustrând legăturile chimice.
Formular pentru înregistrarea compoziției moleculă organică, în care fiecare atom de C este prezentat separat cu legături, se numește c………. f…….. . Atomii de carbon legați chimic reprezintă schelet de carbon molecule de materie.
Trei tipuri de formule structurale
1. Cea mai completă formă de scriere a unei formule de hidrocarburi este atunci când fiecare atom al moleculei este afișat separat:
Acest tip de înregistrare este voluminos, ocupă mult spațiu și este rar folosit.
2.
Formular de înregistrare care indică numărul total atomi de hidrogen la fiecare atom de C, iar liniuțele sunt plasate între atomi de carbon adiacenți,
adică x……… cu…. :
CH 3 –CH 2 –CH 3, Cl–CH 2 –CH 2 –Br.
3. O formulă structurală în care liniuțele dintre atomii aflați într-o înregistrare pe o linie nu sunt indicate, în timp ce atomii care apar pe alte linii sunt conectați prin liniuțe la un lanț drept:
Uneori sunt descrise lanțuri de carbon linii întrerupte, forme geometrice(triunghi, pătrat, cub). În acest caz, la fiecare întrerupere a lanțului, precum și la începutul și sfârșitul lanțului, este implicat un atom de C, de exemplu, în imagini
corespund formulelor structurale
Mai jos sunt câteva proprietăți ale hidrocarburilor saturate individuale și formele lor de înregistrare (Tabelul 1).
tabelul 1
Denumiri de hidrocarburi saturate (alcani) cu structură liniară
| Nume alcan | Molecular formulă | Structural formulă | Agregat stat | Temperatura punctul de fierbere, °C |
|---|---|---|---|---|
| Metan | CH 4 | CH 4 | Gaz | –161,6 |
| Etan | C2H6 | CH 3 CH 3 | Gaz | –88,6 |
| propan | C3H8 | CH 3 CH 2 CH 3 | Gaz | –42,1 |
| Butan | C4H10 | CH 3 CH 2 CH 2 CH 3 | Gaz | –0,5 |
| Pentan | C5H12 | CH3 (CH2)3CH3 | Lichid | 36,1 |
| hexan | C6H14 | CH3(CH2)4CH3 | Lichid | 68,7 |
| heptan | C7H16 | CH3 (CH2)5CH3 | Lichid | 98,5 |
| Octan | C8H18 | CH3 (CH2)6CH3 | Lichid | 125,6 |
| Nonan | C9H20 | CH3(CH2)7CH3 | Lichid | 150,7 |
| Decan | C10H22 | CH3 (CH2)8CH3 | Lichid | 174,0 |
Compilarea denumirilor alcanilor ramificati si substituiti
1. Selectați lanțul de carbon principal și numerotați-l în așa fel (stânga sau dreapta) încât substituenții primiți să primească cele mai mici numere.
2. Numele începe cu un localizant digital - numărul carbonului la care se află substituentul. După număr, numele deputatului este scris printr-o liniuță. Diferiții substituenți sunt enumerați secvenţial. Dacă substituenții identici sunt repeți de două ori, atunci prefixul „di” este scris în nume după localizatorii digitali care indică poziția acestor substituenți. În consecință, cu trei substituenți identici, prefixul este „trei”, cu patru – „tetra”, cu cinci substituenți – „penta”, etc.
Numele supleanților

3. Numele hidrocarburii numerotate ca lanț de carbon principal este scris împreună cu prefixul și substituentul:
a) 2-metilbutan; b) 2,3-dimetilpentan; c) 2-clor-4-metilpentan.
Numele de cicloalcani sunt formate într-un mod similar, numai prefixul „ciclo” este adăugat la numele hidrocarburii - în funcție de numărul de atomi de carbon din ciclu:
Substanțele care sunt similare ca structură, dar diferă în una sau mai multe grupe -CH 2 - sunt cunoscute ca g....... .
Exemple omologi:
CH 3 –CH 3, CH 3 –CH 2 –CH 3, CH 3 –CH 2 –CH 2 –CH 3.
Element de asemănare – alcani cu lanț liniar:
Asemănarea celor trei formule ale substanțelor din ultimul exemplu - în fiecare caz, la al doilea atom de C al lanțului principal de carbon există același substituent - gruparea CH3.
Fenomenul existenței unor substanțe care sunt diferite ca structură și proprietăți, dar au aceeași compoziție calitativă și cantitativă, se numește și……. .
Substanțe care au aceeași m……….. formulă, dar diferite………. formulele sunt......
(Masa 2).
masa 2
Exemple de hidrocarburi izomerice
| Formulă moleculară | Formule structurale |
|---|---|
| C4H10 | CH 3 CH 2 CH 2 CH 3, |
| C5H12 | CH 3 CH 2 CH 2 CH 2 CH 3, |
| C6H14 | CH3 (CH2)4CH3, 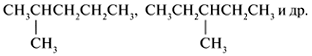
|
Reguli pentru compilarea izomerilor folosind exemplul compusului C5H11CI.
1. Notați lanțul de carbon liniar C5:
S–S–S–S–S.
2. Stabiliți cărei clase de hidrocarburi aparține acest compus. Determinarea se face folosind formule generale pentru hidrocarburi de diferite clase (C n H 2 n+2, C n H 2 nși așa mai departe.). Substanța C5H11Cl este un cloroalcan, adică. este un derivat al unui alcan de forma C n H 2 n+2 (n= 5), în care un atom de H este înlocuit cu Cl. Aceasta înseamnă că toate legăturile din moleculă sunt simple și nu există cicluri.
3. Numerotați atomii de C ai lanțului de carbon (scheletul de carbon) și plasați un heteroatom de Cl la C-1:
4. Notează numărul necesar de atomi de hidrogen la fiecare carbon al lanțului, ținând cont că valența lui C este IV. Rezultatul este izomerul a):
![]()
5. Atomul de clor este mutat de-a lungul lanțului principal C5, conectându-l în serie cu atomii C-2 și C-3. Așa se obțin izomerii b) și c:
O deplasare suplimentară a clorului spre dreapta de-a lungul lanțului nu produce noi izomeri. Astfel, izomerul a*) este identic cu izomerul a), izomerul b*) este identic cu izomerul b). Doar că în izomerii a*) și b*) direcția de numerotare a atomilor de C se schimbă, numărarea se face de la dreapta la stânga (fără asteriscuri era de la stânga la dreapta):
6. Pe baza scheletului de carbon (vezi punctul 3), cel mai exterior (al cincilea) atom de C este îndepărtat și plasat ca substituent pe carbonul intern al lanțului (mai întâi la C-2, apoi la C-3). Lanțurile principale C4 cu un substituent de carbon la C-2 și C-3 se obțin:
Scrieți formulele structurale ale noilor izomeri:
7. Prin plasarea clorului la atomii de C interni ai lanțului principal de carbon C4 se obțin doi izomeri suplimentari:
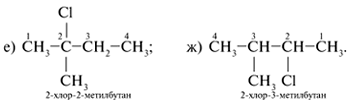
8. O substanță cu formula C 5 H 11 Cl poate avea un lanț principal cu trei atomi de carbon C 3:

Astfel, pentru o substanță cu formula moleculară C 5 H 11 Cl, pot fi compilate opt formule structurale ale izomerilor a)–h) care diferă ca structură.
1.Ce hidrocarburi se numesc nesaturate și cum sunt împărțite? Scrieți formule generale hidrocarburi nesaturate.
Hidrocarburile nesaturate sunt cele care conțin una sau mai multe legături multiple. Principalele clase de hidrocarburi nesaturate sunt alchenele, alchinele și alcadienele.
2. Alchenele includ:
3)
3. Pe baza idei moderne despre orbitalii electronilor, caracterizează natura legăturilor chimice din molecula de etilenă. 
4. Numărul de legături σ dintr-o moleculă de etilenă este egal cu:
2) 5
5. Ce tipuri de izomerie se observă la hidrocarburile saturate și nesaturate? 
6. Desenați formule structurale prescurtate ale tuturor hidrocarburilor a căror formulă moleculară este . Denumiți aceste conexiuni. 
7. De ce este numărul de izomeri în hidrocarburile din seria etilenei mai mare decât în hidrocarburile saturate? Pentru a demonstra acest lucru, dați izomeri de hidrocarburi cu formule moleculare și. 
8. Izomerul pentenei-1 este
3) 2-metilbuten-1
9. Un omolog al propenei este
1) butenă-1
10. Cum sunt produse etilena și hidrocarburile din seria etilenei? Scrieți ecuațiile reacțiilor corespunzătoare. 
11. Ce proprietăți chimice au etilena și omologii ei? Confirmați răspunsul cu ecuații ale reacțiilor corespunzătoare. 
 12. Scrieți ecuațiile pentru reacțiile de ardere ale etilenei și propilenei și interacțiunea acestora cu apa de brom și o soluție de permanganat de potasiu.
12. Scrieți ecuațiile pentru reacțiile de ardere ale etilenei și propilenei și interacțiunea acestora cu apa de brom și o soluție de permanganat de potasiu. 
13. Cum reacţionează propilena şi butenele cu halogenurile de hidrogen? Folosind aceste exemple, explicați esența regulii lui Markovnikov. 
14. În ce scopuri se utilizează etilena și propilena?
Etilena este folosită pentru a produce etilenglicol, polietilenă și alcool etilic. În plus, etilena accelerează coacerea fructelor. Alcoolul izopropilic și polipropilena sunt obținute din propilenă.
15. Ce reacții se numesc reacții de polimerizare? Scrieți ecuația pentru reacția de polimerizare a propilenei. 
16. Scrieți ecuații reacții chimice, confirmând legătura geneticăîntre clase compusi organiciîn diagrama 5. 
 Problema 1. Calculați:
Problema 1. Calculați:
a) ce volum și ce masă de etilenă se poate obține din 160 ml alcool etilic, a cărui densitate este de 0,8 g/cm3; b) ce volum de alcool etilic absolut (anhidru) (ρ=0,8 g/cm3) se poate obține din 100 m3 de etilenă (n.s.) 
 Problema 2. La trecerea etilenei prin apa cu brom masa soluției a crescut cu 7 g Ce volum de gaz a reacționat și ce masă de 1,2-dibrometan s-a format (nr.)?
Problema 2. La trecerea etilenei prin apa cu brom masa soluției a crescut cu 7 g Ce volum de gaz a reacționat și ce masă de 1,2-dibrometan s-a format (nr.)? 
Problema 3. Ce volum de etilenă (nr.) va fi necesar pentru a produce 126 kg de oxid de etilenă, dacă fractiune in masa pierderile de producție de etilenă este de 0,1? 
Problema 4. Ce volum de aer este necesar pentru a arde 50 de litri de propilenă (n.o.)? 
1. Scrieți formulele structurale ale izomerilor compușilor carbonilici cu formula generală c5h10o și denumiți-le după nomenclatura rațională, nomenclatura Iupak.
Soluţie:
Pentru compușii carbonilici, formarea de izomeri structurali este asociată cu o modificare a structurii lanțului de carbon, o aranjare diferită a grupării carbonil în lanțul de carbon:
Gruparea funcțională din formulele structurale ale aldehidelor este adesea scrisă sub forma unei formule prescurtate ca CHO (COH - incorect!), în cetone atomul de oxigen este plasat în paranteze (O).
2. Scrieți ecuațiile de reacție pentru oxidarea butanalului și a 2-metilpentanonei-3 cu un amestec de crom.
Soluţie:
Când aldehidele sunt oxidate, se formează acizi carboxilici fără modificarea numărului de atomi de carbon din compoziția lor. Oxidarea cetonelor este însoțită de distrugerea lanțului de carbon, ducând la formarea unui amestec de acizi carboxilici și (sau) cetone cu un număr mai mic de atomi de carbon (comparativ cu cetona originală) în compoziția lor:

3. Scrieți schemele de reacție pentru acetonă și acetaldehidă cu acidul cianhidric și hidroxilamină. Comparați reactivitatea compușilor carbonilici în aceste reacții.
Soluţie:
Interacțiunile acetonei și acetaldehidei cu acești reactivi se referă la reacții de adiție nucleofile (AN). Schemele de reacție arată astfel:
a) interacţiunea cu acidul cianhidric


Hidroliza oxinitrililor rezultați este însoțită de formarea de α - hidroxiacizi, iar numărul de atomi de carbon din compoziția acidă crește cu unul: acid 2-hidroxipropanoic
(acid lactic)
b) interacțiunea cu hidroxilamina:

Reacţiile de adiţie nucleofilă cu nucleofili conţinând azot (NH3, NH2OH, NH2-NH2 etc.) sunt însoţite de eliminarea ulterioară a unei molecule de apă din produsul de reacţie.
Reactivitatea aldehidelor în aceste reacții este mai mare decât cea a cetonelor, deoarece mărimea sarcinii pozitive pe atomul de carbon al grupării carbonil din aldehide în comparație cu cetonele este mai mare:
|
|
|
4. Obțineți acetonă folosind toate metodele posibile.
Soluţie:
Compușii carbonilici pot fi obținuți ca rezultat al următoarelor transformări:
1. hidroliza hidrocarburilor dihalogenate de 33 mm:

2. oxidarea alcoolilor, în care aldehidele se formează din alcooli primari și cetonele din alcoolii secundari:

3. ozonoliza alchenelor urmată de hidroliză:

4. hidratarea alchinelor (reacția Kucherov):

5. piroliza sărurilor de calciu (bariu) ale acizilor carboxilici:
3.3. Acizi carboxilici și derivații lor
Literatură
1. Ivanov, V.G. Chimie organica: manual manual pentru universități / V.G. Ivanov, V.A. Gorlenko. – M.: Centrul de Editură „Academia”, 2009. -P. 222-254.469-479.
2. Grandberg, I.I. Chimie organică: manual. pentru universități / I.I. Grandberg. - M.: Butarda, 2002. -S. 357-392, 410-426, 393-399.
3. Artemenko, A.I. Chimie organică: manual. pentru universități / A.I. Artemenko. - M.: facultate, 2009. -P.170-199, 251-253, 259-272, 402-408.
4. Petrov, A.A. Chimie organică: manual. pentru universități / A.A. Petrov. - Sankt Petersburg: Ivan Fedorov, 2002. -S. 189-2003, 207-220, 257-285, 421-434.
Manualele recomandate prezintă un volum de material semnificativ mai mare decât este necesar pentru program. Toate manualele discută în detaliu structura electronică, proprietățile chimice ale acizilor carboxilici, prepararea și utilizarea acizilor și a derivaților acestora. În manualul recomandat, materialul este prezentat sistematic și pe scurt, deci este mai bine să studiați în mod independent subiectul „Acizi carboxilici și derivații lor” folosind manualul.
Derivații de hidrocarburi care conțin o grupare carboxil se numesc acizi carboxilici.
Studiul acizilor carboxilici ar trebui să înceapă cu luarea în considerare a grupului carboxil și a clasificării generale a acizilor. În funcție de natura radicalului și de numărul de grupe carboxilice, există mai multe tipuri de acizi carboxilici: acizi carboxilici alifatici și aromatici, acizi mono și dicarboxilici, precum și cu funcții mixte - hidroxi, oxo și aminoacizi. .
La studierea nomenclaturii, trebuie remarcat faptul că cele mai comune sunt denumirile banale ale acizilor trebuie amintite unele denumiri: acetic (etan), butiric (butan), oleic, stearic, linoleic, tartric, oxalic etc. Principiile compilării denumirilor acizilor conform nomenclaturii IUPAC au fost discutate mai devreme (vezi „Nomenclatura compușilor organici”).
Când studiezi proprietăți fizice acizi carboxilici, trebuie acordată atenție formării legăturilor de hidrogen intermoleculare.
Când studiezi proprietăți chimice acizi, este necesar să se stabilească asemănări cu acizii anorganici: capacitatea de disociere, formarea de săruri Prezența unui atom de hidrogen mobil în grupa carboxil -COO N defineste proprietăți acide acizi carboxilici. Puterea acizilor depinde de o serie de factori: structura și compoziția radicalului, prezența grupărilor de atragere sau donatoare de electroni în radical, numărul de grupări carboxil etc. Ca rezultat al interacțiunii cu metale, oxizi de metal, baze și unele săruri, acizii formează săruri. Ar trebui să luați în considerare proprietățile sărurilor de sodiu și calciu (solubilitate, relație cu hidroliză, încălzire), să acordați atenție sărurilor acizilor carboxilici superiori (săpunuri).
Acizii carboxilici sunt caracterizați prin reacții de substituție nucleofilă. Înlocuirea grupării hidroxil în grupa carboxil duce la producerea derivaților acizi: anhidride, halogenuri acide, amide, esteri. Elevul ar trebui să acorde o atenție deosebită reacției de esterificare (chitanță esteri), condițiile și mecanismul acestuia. Când studiem chimia grăsimilor, este necesar să ne amintim formulele a cinci acizi bazici (2 saturati și 3 nesaturați) și alcoolul trihidroxilic - glicerol, care fac parte din trigliceride. Ar trebui să înveți să scrii ecuații de reacție pentru formarea grăsimilor și să înveți cele mai importante proprietăți chimice ale grăsimilor: hidroliza, hidrogenarea.
O proprietate comună a tuturor derivaților acizi este hidroliza lor (acidă și alcalină), care are ca rezultat formarea unui acid carboxilic sau a sării acestuia. Derivații acizilor sunt utilizați pe scară largă în sinteza organică pentru acilarea alcoolilor, fenolilor, aminelor și a altor compuși.
Când se studiază acizii dicarboxilici, este necesar să se observe atât asemănarea, cât și diferența cu acizii monocarboxilici, datorită numărului mare de grupări carboxilice și influenței lor reciproce.
Când se studiază structura și proprietățile chimice ale acizilor nesaturați, este necesar să se repete materialul studiat anterior asupra hidrocarburilor nesaturate (a se vedea „Alchenele”).
Când studiați hidroxiacizii, ar trebui să acordați atenție izomeriei optice caracteristice acestor compuși, să luați în considerare proprietățile acizilor din grupa carboxil (formarea de săruri, esteri) și gruparea alcoolului (substituirea grupei OH, formarea de alcoolați, eteri și esteri). Este necesar să se ia în considerare relația hidroxiacizilor cu încălzirea și eliminarea apei cu formarea de produse de diferite structuri.
Acizii ceto pot fi luați în considerare folosind exemplul acizilor piruvic și acetoacetic. Acidul piruvic este un produs intermediar important în conversia carbohidraților și proteinelor în organism; este necesar să se țină cont de existența formelor enol și cetonice ale acidului.
Principalele metode de producere a acizilor carboxilici: hidroliza derivaților acestora (nitrili, esteri etc.), oxidarea alchenelor, alcoolilor și aldehidelor, fermentarea carbohidraților etc.
Întrebări și exerciții de testare:
1. Scrieți formulele structurale ale tuturor acizilor izomeri din compoziția C 5 H 10 O 2. Numiți compușii folosind nomenclaturi triviale și substitutive. Comparați proprietățile acide ale izomerilor.
2. Scrieți pentru acidul propionic (propanoic) ecuațiile pentru posibilele reacții cu sodiu metalic, hidroxid de cupru (II), carbonat de sodiu, alcool etilic, amoniac, urmate de încălzire. Numiți compușii rezultați folosind nomenclatura IUPAC.
3. Scrieți formulele structurale ale acizilor dicarboxilici izomeri cu compoziția C 4 H 6 O 4. Numiți izomerii rezultați.
4. Scrieți formulele structurale ale acizilor nesaturați izomeri cu compoziția C 4 H 6 O 2. Care dintre ele va avea izomeri geometrici? Numiți izomerii structurali și spațiali.
5. Scrieți formula structurală a trigliceridei - dipalmitooleina. Scrieți ecuațiile pentru bromurare, saponificare cu hidroxid de sodiu, oxidare cu permanganat de potasiu a grăsimii indicate.
6. Comparați proprietățile acide ale acizilor acetic, oxoacetic, oxalic și hidroxiacetic.
EXEMPLE DE SOLUȚII LA PROBLEME TIPICE
| " |


 >
>